In uno studio pubblicato su Nature Materials, gli scienziati dell’Università di Stuttgart hanno presentato un nuovo approccio per manipolare le cellule sintetiche utilizzando nanorobot di DNA riconfigurabili. Questa ricerca collega il mondo nanoscopico a quello microscopico, offrendo un metodo sofisticato per rimodellare le membrane cellulari e creare canali sintetici funzionali, con il potenziale di rivoluzionare la biologia sintetica.
Il ruolo della forma nella funzione cellulare
Nei sistemi biologici, la forma delle cellule e dei loro componenti gioca un ruolo cruciale nel facilitare le interazioni e mantenere la funzionalità. La membrana plasmatica, una struttura cellulare vitale, combina lipidi e proteine per formare una barriera flessibile ma controllata. Mentre le proteine regolano il trasferimento molecolare, sia i lipidi che le proteine contribuiscono alla morfologia della cellula, influenzandone le interazioni con l’ambiente. La biologia sintetica mira a emulare queste caratteristiche costruendo modelli cellulari funzionali da zero.
Tuttavia, ottenere un controllo dinamico della forma nelle cellule sintetiche rimane una sfida. Le cellule biologiche si rimodellano e rispondono continuamente agli stimoli, mentre gli analoghi sintetici spesso mancano di questa adattabilità. Il nuovo studio affronta questa limitazione introducendo strumenti a base di DNA capaci di indurre cambiamenti morfologici programmabili e reversibili.
Nanorobot di DNA: uno strumento nanoscopico per il controllo su scala microscopica
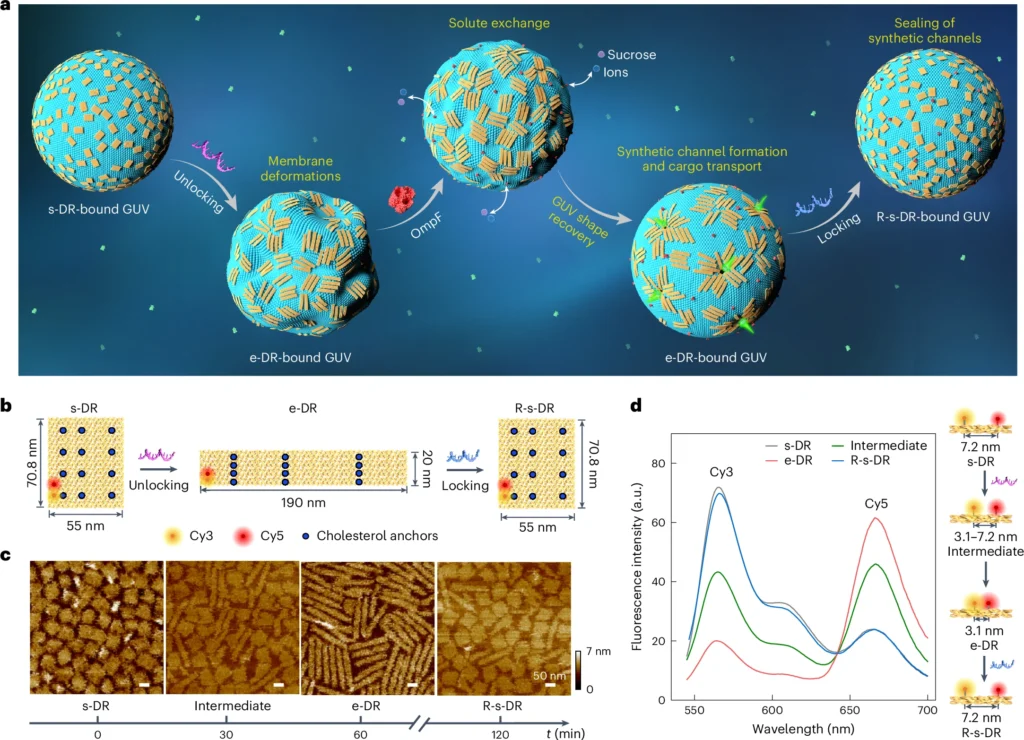
Al centro di questa innovazione ci sono i nanoraft di DNA, strutture create utilizzando tecniche di “DNA origami”. Questi nanoraft sono progettati per passare da una forma all’altra, come da una forma quadrata a una rettangolare allungata, attraverso interazioni specifiche con sequenze di DNA. Questa transizione non ha semplicemente un impatto estetico: essa, infatti, modifica attivamente le membrane delle cellule sintetiche a cui sono agganciati.
Il sistema utilizza vescicole unilamellari giganti (GUV) come modelli di cellule sintetiche. Quando i nanoraft di DNA si legano alla membrana della vescicola, i loro cambiamenti strutturali creano una pressione sterica che deforma la superficie della GUV. Il risultato è un’interazione sorprendente, in cui i cambiamenti nanoscopici nella configurazione del DNA si traducono direttamente in trasformazioni microscopiche nella forma della cellula sintetica.
È importante ricordare che queste trasformazioni morfologiche sono reversibili. In altre parole, introducendo specifiche sequenze di DNA, i nanoraft possono tornare alla loro forma originale, consentendo alle GUV di recuperare la loro forma sferica. Questa funzionalità reversibile permette un livello di precisione e controllo finora mai raggiunto nell’ingegneria delle cellule sintetiche.
Canali sintetici: una nuova frontiera nella funzionalità delle membrane
Uno dei risultati più significativi di questo studio è la creazione di canali sintetici all’interno delle membrane delle GUV. Quando i nanoraft di DNA si auto-organizzano in domini ordinati, perforano la membrana, formando canali funzionali. Questi canali consentono il trasporto di molecole, comprese entità più grandi come la proteina fluorescente verde (GFP), attraverso la membrana.
La capacità di regolare la permeabilità della membrana con tale precisione rappresenta un progresso notevole. Inoltre, i canali sintetici formati dai nanoraft di DNA possono essere sigillati e riaperti su richiesta. Questa caratteristica consente un trasporto controllato del carico, una capacità che supera le limitazioni dei pori naturali a base proteica.
Esplorare la dinamica dei nanoraft di DNA e delle GUV
I ricercatori hanno esaminato attentamente i parametri che influenzano le interazioni tra i nanoraft di DNA e le GUV. Fattori come la densità dei nanoraft, la configurazione degli ancoraggi di colesterolo e la pressione osmotica hanno un ruolo fondamentale nel determinare l’entità della deformazione delle GUV e la formazione dei canali. In condizioni ottimali, i nanoraft di DNA inducono cambiamenti significativi, evidenziando l’importanza di ottimizzare queste variabili per ottenere la massima efficienza.
I canali stessi dimostrano di avere una dimensione compatibile con il trasporto di molecole fino a 70 kilodalton e questa capacità li rende strumenti versatili per molteplici applicazioni. Il sistema ha inoltre dimostrato stabilità e adattabilità, garantendo la funzionalità dei canali per periodi prolungati.
Applicazioni e implicazioni
La capacità di rimodellare le cellule sintetiche e regolarne la funzionalità apre la strada verso numerose possibilità nella biotecnologia e nella medicina. Il trasporto controllato di carichi attraverso canali sintetici può essere applicato nei sistemi di somministrazione di farmaci, dove gli agenti terapeutici vengono rilasciati direttamente nelle aree bersaglio. Allo stesso modo, il rimodellamento dinamico delle membrane potrebbe essere utilizzato su piattaforme di biosensori, consentendo un adattamento in tempo reale ai cambiamenti ambientali.
Oltre alle applicazioni biomediche, questa tecnologia ha anche implicazioni per la ricerca di base. Ricreando e superando i processi cellulari naturali, gli scienziati possono ottenere una comprensione più profonda dei meccanismi alla base della vita, progettando al contempo funzionalità completamente nuove. Inoltre, la modularità dei nanoraft di DNA consente di raggiungere un livello di personalizzazione tale da permette ai ricercatori di adattare le cellule sintetiche a compiti specifici.
Sfide e prospettive future
Nonostante le sue potenzialità, la tecnologia presenta anche diverse sfide. La stabilità delle nanostrutture di DNA in ambienti biologici complessi e la scalabilità per applicazioni su larga scala restano ancora aspetti da studiare. Inoltre, l’integrazione di questi sistemi con le piattaforme biotecnologiche esistenti richiede ulteriori sviluppi.
Ciononostante, lo studio rappresenta un passo avanti significativo. Combinando la programmabilità della nanotecnologia a DNA con la versatilità della biologia sintetica, questa ricerca pone le basi per futuri progressi. La possibilità di progettare cellule sintetiche dinamiche e funzionali, in grado di interagire con l’ambiente in modi nuovi e senza precedenti, evidenzia l’impatto trasformativo di questo approccio.

Lascia un commento